11/10/2023
El término "radiactividad" a menudo evoca imágenes de peligro y misterio. Desde su descubrimiento a finales del siglo XIX, ha transformado nuestra comprensión de la materia y la energía, dando lugar a aplicaciones que van desde la medicina hasta la generación de electricidad. Pero, ¿alguna vez te has preguntado cuál es el elemento más radiactivo o la sustancia más potente en términos de emisión de radiación? La respuesta no es tan simple como nombrar un único elemento, ya que depende de si hablamos de abundancia natural, potencia por gramo o las implicaciones de su manejo. Acompáñanos a desentrañar este enigma y conocer a los protagonistas del mundo radiactivo.

¿Qué es la Radiactividad?
Para entender qué hace que un elemento sea radiactivo, primero debemos comprender el concepto fundamental. La radiactividad es un fenómeno natural por el cual los núcleos atómicos inestables de ciertos elementos emiten partículas (alfa o beta) y/o energía (radiación gamma) para transformarse en núcleos más estables. Este proceso de transformación se conoce como decaimiento radiactivo.
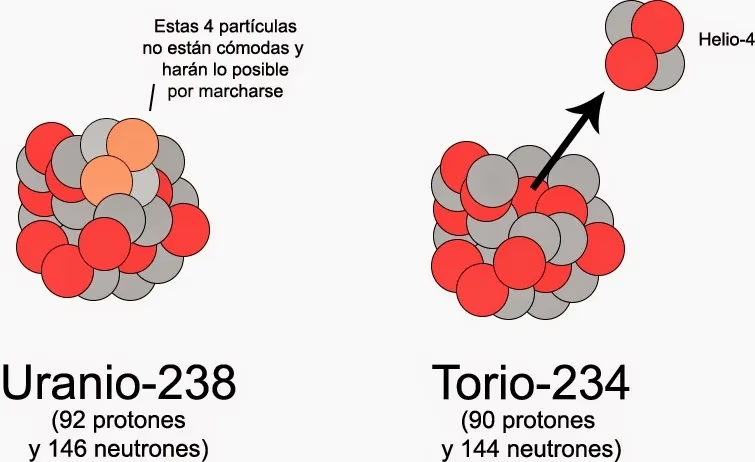
Cada elemento químico puede tener diferentes isótopos, que son átomos con el mismo número de protones pero distinto número de neutrones. Algunos isótopos son estables, mientras que otros son inestables y, por lo tanto, radiactivos. La naturaleza de la radiación emitida (alfa, beta o gamma) determina su capacidad de penetración y el tipo de daño que puede causar.
Fuentes Naturales de Radiactividad: Uranio y Torio
Cuando exploramos las fuentes naturales de radiactividad en nuestro planeta, dos nombres emergen como los más destacados en términos de abundancia en la corteza terrestre: el Uranio y el Torio.
La Abundancia en la Tierra
El Uranio es un elemento químico radiactivo que se encuentra de forma natural. Con número atómico 92 y símbolo U, pertenece al grupo de los actínidos. Es sorprendentemente abundante en la corteza terrestre, superando al oro en volumen unas 500 veces. Se halla en rocas, suelo, agua e incluso en pequeñas cantidades en el cuerpo humano. Los océanos, por ejemplo, contienen miles de millones de toneladas de uranio diluido.
El Uranio se presenta principalmente como isótopos Uranio-238 (238U) y Uranio-235 (235U). Junto con el Torio, que existe mayoritariamente como Torio-232 (232Th), estos elementos son fundamentales no solo en la historia geológica de la Tierra, sino también como combustible clave en la tecnología nuclear moderna. Una pequeña cantidad de uranio puede generar una enorme cantidad de energía; una porción del tamaño de un huevo de gallina puede producir la misma electricidad que 88 toneladas de carbón.
El Concepto de Vida Media
La persistencia del Uranio y el Torio a lo largo de miles de millones de años se debe a sus extremadamente largas vidas medias. La vida media es el tiempo que tarda la mitad de los átomos de un isótopo radiactivo en decaer o transformarse en otro elemento o isótopo. Es un concepto fundamental para entender la longevidad de la presencia de un elemento radiactivo.
Las vidas medias del 238U, 235U y 232Th son de aproximadamente 4.500 millones de años, 700 millones de años y 14.000 millones de años, respectivamente. Estas cifras colosales significan que, incluso después de miles de millones de años, una fracción significativa de la cantidad original de estos isótopos aún no ha decaído, actuando como guardianes de la radiactividad terrestre a lo largo de las eras geológicas.
El Polonio-210: Una Sustancia de Extrema Potencia
Si bien el Uranio y el Torio son los elementos radiactivos más abundantes en la naturaleza, la pregunta sobre la sustancia "más radiactiva" a menudo se refiere a la potencia de la radiación emitida por unidad de masa o la peligrosidad de la sustancia en pequeñas cantidades. En este contexto, el Polonio-210 (210Po) es un protagonista notorio.

El Polonio es un elemento químico radiactivo descubierto por Pierre y Marie Curie en 1898, extraído de la pechblenda (uraninita). Existen 27 isótopos de polonio, pero el 210Po es uno de los que se encuentra en la naturaleza y es extremadamente difícil de manejar.
Lo que distingue al 210Po es su elevada actividad específica, es decir, la cantidad de desintegraciones por segundo por unidad de masa. Se menciona que es 50 veces más radiactivo que el uranio. Aunque su vida media es relativamente corta (alrededor de 138 días) comparada con el Uranio o Torio, esta corta vida media implica una tasa de decaimiento (y por lo tanto de emisión de radiación) muy alta en el momento de su formación o aislamiento. Es esta alta tasa de emisión de partículas alfa lo que lo hace increíblemente peligroso incluso en cantidades minúsculas.
El 210Po suele presentarse como un polvo rojo en forma de óxido. Es indetectable por los sentidos humanos y requiere guantes de plomo y ambientes especiales para su manejo seguro en entornos industriales o de investigación atómica. La ingesta o inhalación de tan solo medio miligramo puede ser mortal debido a la radiación interna que emite. Sus efectos, aunque no inmediatos, son devastadores, afectando órganos vitales y la médula ósea, llevando a un fallo multiorgánico similar a una exposición masiva por radiación, pero de forma localizada e interna.
El caso del envenenamiento de Alexander Litvinenko con 210Po en 2006 puso de manifiesto la extrema toxicidad y la dificultad de detección de esta sustancia si se administra subrepticiamente.
Medición y Unidades de la Radiactividad
Para cuantificar la radiactividad y sus efectos, se utilizan diversas unidades. La unidad del Sistema Internacional (SI) para la actividad radiactiva (el número de desintegraciones por segundo) es el becquerel (Bq), que equivale a una desintegración por segundo. Una unidad más antigua y aún utilizada es el curie (Ci), donde 1 Ci = 3.7 × 1010 Bq.
Sin embargo, la actividad por sí sola no indica el riesgo para la salud, ya que este depende de la energía depositada y el tipo de radiación. Para medir la energía absorbida por un material, se usa el gray (Gy). Y para evaluar el daño biológico en tejidos vivos, se utiliza el sievert (Sv), que pondera la dosis absorbida (en Gray) según el tipo de radiación (alfa, beta, gamma) y la sensibilidad del tejido.
Un instrumento común para detectar la radiactividad es el contador Geiger, que registra los impulsos eléctricos generados cuando las partículas radiactivas ionizan un gas dentro de un tubo.
Riesgos para la Salud y Protección Radiológica
La exposición a la radiación ionizante conlleva riesgos para la salud que dependen de varios factores: la intensidad de la radiación, la duración de la exposición, el tipo de radiación y la parte del cuerpo afectada.
La Dosis y sus Efectos
Los efectos de la radiación se relacionan con la dosis absorbida, medida en Sieverts (Sv) o milisieverts (mSv). Las radiaciones alfa y beta son peligrosas principalmente si la fuente está dentro del cuerpo (por ingestión o inhalación), mientras que las radiaciones gamma y X son peligrosas tanto interna como externamente debido a su alto poder de penetración.
Se considera que una dosis efectiva de 100 mSv en un año puede empezar a producir efectos detectables en el organismo. Sin embargo, existen límites de exposición establecidos para proteger a la población y a los trabajadores ocupacionalmente expuestos.
Límites de Exposición Aceptables
La protección radiológica busca mantener las dosis tan bajas como sea razonablemente posible. Los métodos clave para reducir la exposición son: 1) reducir el tiempo de exposición, 2) aumentar la distancia a la fuente y 3) utilizar blindajes adecuados.
Existen límites legales de dosis efectiva. En la Unión Europea, el límite para trabajadores expuestos es de 100 mSv en un período de cinco años consecutivos, con un máximo de 50 mSv en un solo año. Para la población general, el límite es mucho más estricto: 1 mSv por año, además del fondo natural (que promedia unos 2.4 mSv al año a nivel mundial). Estos límites se basan en modelos de riesgo y buscan asegurar un nivel de riesgo considerado aceptable.
En entornos controlados, como centrales nucleares, se delimitan zonas con diferentes niveles de radiación permitida y acceso restringido:
| Zona | Tasa de Dosis (mSv/h) |
|---|---|
| Zona gris o azul | 0,0025 a 0,0075 |
| Zona verde | 0,0075 a 0,025 |
| Zona amarilla | 0,025 a 1 |
| Zona naranja | 1 a 100 |
| Zona roja | > 100 |
En situaciones de emergencia radiológica, los límites pueden ser superiores para permitir acciones urgentes, pero siempre intentando minimizar la dosis recibida.
La Ley de Radiosensibilidad
No todos los tejidos del cuerpo son igual de sensibles a la radiación. La ley de Bergonié y Tribondeau (1906) establece que los tejidos y órganos más sensibles son aquellos menos diferenciados y con alta actividad reproductiva. Ejemplos de tejidos altamente radiosensibles incluyen el epitelio intestinal, órganos reproductores, médula ósea y glándula tiroides. Las neuronas y el hueso, por ejemplo, son considerablemente menos sensibles.
Ejemplos de Isótopos Radiactivos
Además del Uranio, Torio y Polonio-210, existen muchos otros isótopos radiactivos, tanto naturales como creados por el ser humano:
Isótopos Naturales
Entre los isótopos radiactivos que se encuentran de forma natural, además de los ya mencionados 235U, 238U, 232Th y 210Po, destacan el Radio (226Ra, 228Ra), el Carbono-14 (14C), el Tritio (3H), el Radón (222Rn) y el Potasio-40 (40K). Estos contribuyen al "fondo natural" de radiación al que estamos expuestos diariamente.

Isótopos Artificiales
La actividad humana, especialmente en medicina, industria y generación de energía nuclear, ha creado o concentrado isótopos artificiales. Algunos ejemplos importantes son el Plutonio (239Pu, 241Pu), Curio (242Cm, 244Cm), Americio (241Am), Cesio (134Cs, 135Cs, 137Cs), Yodo (129I, 131I, 133I), Antimonio-125 (125Sb), Rutenio-106 (106Ru), Estroncio-90 (90Sr), Kriptón (85Kr, 89Kr), Selenio-75 (75Se) y Cobalto-60 (60Co), así como el Cloro-36 (36Cl).
Preguntas Frecuentes (FAQ)
P: ¿Es peligroso el Uranio si lo encuentro en la naturaleza?
R: El Uranio natural emite principalmente partículas alfa, que tienen un bajo poder de penetración y pueden ser detenidas por una hoja de papel o la piel. El riesgo principal del Uranio natural radica en la exposición interna (por ingestión o inhalación de polvo) o en su toxicidad química, más que en su radiactividad externa. En concentraciones bajas y naturales, el riesgo radiológico es bajo.
P: ¿Cuál es la diferencia entre Becquerel y Sievert?
R: El Becquerel (Bq) mide la actividad radiactiva, es decir, cuántos átomos se desintegran por segundo en una fuente. El Sievert (Sv) mide la dosis efectiva, que representa el riesgo biológico para la salud humana, teniendo en cuenta el tipo de radiación, la energía y la sensibilidad de los tejidos irradiados. Una alta actividad (Bq) no siempre significa una alta dosis (Sv) si la radiación emitida es poco penetrante o la fuente está lejos.
P: ¿Cómo me protejo de la radiación?
R: Las medidas básicas de protección radiológica son: tiempo (minimizar la duración de la exposición), distancia (alejarse de la fuente, ya que la intensidad disminuye rápidamente con la distancia) y blindaje (interponer materiales absorbentes entre la fuente y la persona, como plomo, hormigón o agua, dependiendo del tipo de radiación).
P: ¿Todos los elementos radiactivos son artificiales?
R: No, existen muchos isótopos radiactivos que se encuentran de forma natural en el medio ambiente desde la formación de la Tierra (como el Uranio y el Torio) o que se producen continuamente (como el Carbono-14 y el Tritio por interacción con la radiación cósmica, o el Radón por decaimiento del Radio). Sin embargo, muchos otros isótopos radiactivos se producen artificialmente en reactores nucleares o aceleradores de partículas para diversas aplicaciones.
P: Si el Polonio-210 es tan peligroso, ¿por qué se utiliza?
R: A pesar de su peligrosidad, el Polonio-210 tiene usos específicos en cantidades muy pequeñas y bajo estrictas medidas de seguridad. Por ejemplo, se ha utilizado en fuentes de energía termoeléctrica para satélites o sondas espaciales (debido al calor que genera su decaimiento) y en dispositivos antiestáticos industriales.
Conclusión
Definir el "elemento más radiactivo" no es tan simple como parece. Si consideramos la abundancia natural a gran escala, el Uranio y el Torio encabezan la lista. Si pensamos en la potencia por gramo y la peligrosidad en cantidades mínimas, sustancias como el Polonio-210 demuestran una radiactividad específica extraordinariamente alta. Lo crucial es comprender que la radiactividad es un fenómeno complejo que requiere conocimiento para su manejo seguro y su aprovechamiento en diversas áreas. La ciencia nos permite medirla, entender sus efectos y establecer medidas de protección para convivir con esta poderosa fuerza de la naturaleza de la manera más segura posible.
Si quieres conocer otros artículos parecidos a ¿Cuál es el Elemento Más Radiactivo? puedes visitar la categoría Sofas.
