13/04/2026
El Síndrome de Respuesta Inflamatoria Sistémica (SIRS) representa una respuesta de defensa exagerada del cuerpo ante un factor estresante nocivo. Este factor puede ser una infección, un trauma, una cirugía, una inflamación aguda, isquemia o reperfusión, o una malignidad, entre otros. El objetivo de esta respuesta es localizar y luego eliminar la fuente endógena o exógena del insulto. En el corazón del escenario clínico se encuentra una desregulación en la homeostasis de las vías proinflamatorias y antiinflamatorias, con la liberación desregulada de reactantes de fase aguda y crónica.

Aunque la intención es defensiva, la tormenta de citoquinas desregulada puede causar una cascada inflamatoria masiva que conduce a disfunción orgánica reversible o irreversible e incluso a la muerte. El SIRS con una fuente de infección sospechada se denomina sepsis. Por lo tanto, la confirmación de la infección con cultivos positivos no es obligatoria, al menos en las etapas tempranas. La sepsis con una o más fallas orgánicas se llama sepsis grave, y la inestabilidad hemodinámica a pesar de la reposición del volumen intravascular se llama shock séptico. Juntos, representan un continuo fisiológico con un empeoramiento progresivo del equilibrio entre las respuestas proinflamatorias y antiinflamatorias del cuerpo.
Criterios de Definición del SIRS
Objetivamente, el SIRS se define por la satisfacción de al menos dos de los siguientes criterios:
| Criterio | Descripción |
|---|---|
| Temperatura Corporal | Mayor de 38 °C o menor de 36 °C. |
| Frecuencia Cardíaca | Mayor de 90 latidos/minuto. |
| Frecuencia Respiratoria | Mayor de 20 respiraciones/minuto o presión parcial de CO2 menor de 32 mmHg. |
| Recuento de Leucocitos | Mayor de 12000 o menor de 4000 /microlitros o más del 10% de formas inmaduras o bandas. |
En la población pediátrica, la definición se modifica para requerir obligatoriamente un recuento anormal de leucocitos o temperatura para establecer el diagnóstico, ya que las frecuencias cardíacas y respiratorias anormales son más comunes en niños. En resumen, casi todos los pacientes sépticos tienen SIRS, pero no todos los pacientes con SIRS son sépticos.
Historia y Evolución de la Definición
Con la llegada de nuevos conceptos en la fisiopatología e intervenciones terapéuticas para la sepsis a principios de los años 90, surgió una creciente necesidad de identificar un grupo homogéneo de sujetos potenciales para ensayos clínicos que investigaran nuevas estrategias terapéuticas innovadoras. De la plétora de estudios emergentes, una opinión fue unánime: se necesita un enfoque temprano y sensible al tiempo para el diagnóstico y la intervención para impactar significativamente la supervivencia y la morbilidad del paciente. La identificación de los sujetos en cualquier entorno con parámetros estandarizados y fáciles de usar, por lo tanto, fue clave. La conferencia de consenso sobre definiciones de sepsis patrocinada por el American College of Chest Physicians/Society of Critical Care Medicine, celebrada en Chicago, Illinois, en agosto de 1991, tuvo como objetivo establecer un grupo estándar de parámetros clínicos para identificar fácilmente a esos sujetos en cualquier entorno clínico. Así nació la definición de SIRS.
Esta definición sufrió una nueva modificación en el segundo capítulo de la reunión en 2001 en Washington, DC. Esta conferencia propuso un marco conceptual para la estadificación de la sepsis utilizando el acrónimo PIRO (predisposición, insulto o infección, respuesta y disfunción orgánica). El objetivo de la definición inicial era ser altamente sensible utilizando parámetros fácilmente disponibles en todos los entornos de atención médica. Una consecuencia inevitable de tal definición fue, por lo tanto, la falta de especificidad.
Algunas de las limitaciones más relevantes de la definición de SIRS, señaladas en la literatura, incluyen:
- La prevalencia universal de los parámetros en un entorno de UCI.
- Falta de capacidad para distinguir entre una respuesta beneficiosa del huésped y una respuesta patológica del huésped que contribuye a la disfunción orgánica.
- Distinguir entre etiología infecciosa y no infecciosa basándose únicamente en la definición.
- Falta de peso para cada criterio – por ejemplo, la fiebre y la frecuencia respiratoria elevada tienen exactamente la misma significancia que la leucocitosis o la taquicardia según la definición de SIRS.
- Incapacidad para predecir la disfunción orgánica.
En un estudio de más de 130,000 pacientes sépticos, se estableció que uno de cada ocho pacientes no cumplía con dos o más criterios SIRS al ingreso, pero progresaba a infección grave y disfunción multiorgánica y muerte. También se estableció que cada criterio en la definición de SIRS no se traduce en un riesgo equivalente de disfunción orgánica o muerte.
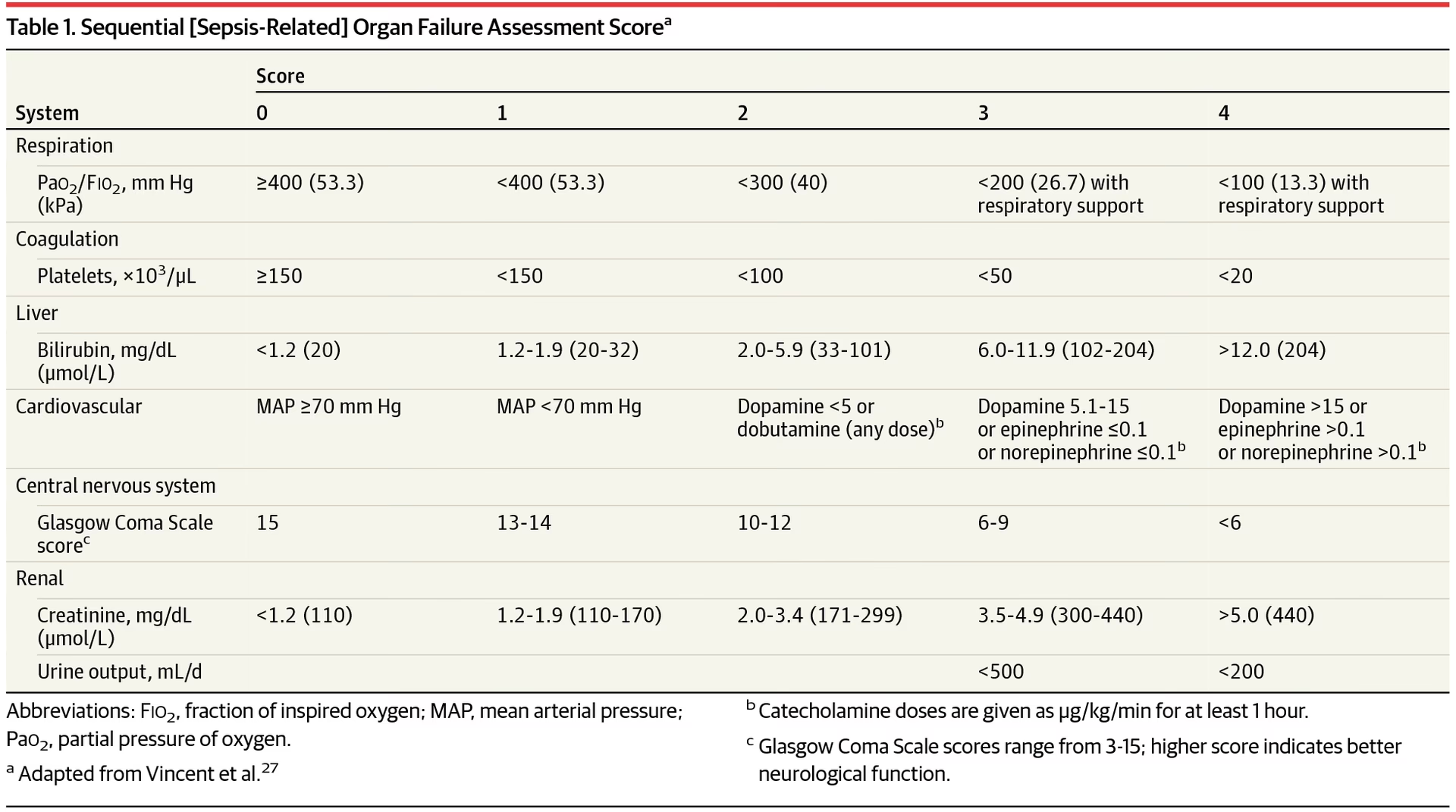
A raíz de este debate, en 2016, la European Society of Intensive Care Medicine y la Society of Critical Care Medicine (SCCM) crearon un grupo de trabajo que propuso Sepsis-3, una nueva definición para la sepsis. La nueva definición excluyó el establecimiento de los criterios SIRS para definir la sepsis y la hizo más inespecífica como cualquier disfunción orgánica potencialmente mortal causada por la respuesta desregulada del huésped a la infección. El grupo de trabajo afirmó que la evaluación de la falla orgánica secuencial (SOFA) tiene una mejor validez predictiva para la sepsis que los criterios SIRS. Tiene una mejor precisión pronóstica y la capacidad de predecir la mortalidad hospitalaria. Para reducir la complejidad del cálculo del SOFA, introdujeron el qSOFA.
El qSOFA es un sistema de evaluación de 3 componentes:
- Presión arterial sistólica por debajo de 100 mm Hg.
- Frecuencia respiratoria más alta que excede las 21.
- Puntuación más baja de la escala de coma de Glasgow es inferior a 15.
Aunque la validez del qSOFA es limitada en un entorno de UCI, ha superado consistentemente a los criterios SIRS en la predicción de la disfunción orgánica en un entorno no UCI y de urgencias.
Etiología del SIRS
A nivel molecular, la etiopatogenia del síndrome de respuesta inflamatoria sistémica se divide ampliamente en Patrones Moleculares Asociados a Daño (DAMP) y Patrones Moleculares Asociados a Patógenos (PAMP).
Aunque la lista no es exhaustiva, algunas etiologías comunes desde una perspectiva clínica incluyen:
Patrones Moleculares Asociados a Daño (DAMP)
- Quemaduras
- Trauma
- Trauma relacionado con procedimientos quirúrgicos
- Aspiración aguda
- Pancreatitis aguda
- Abuso de sustancias e intoxicaciones relacionadas
- Isquemia de órgano terminal aguda
- Exacerbación aguda de vasculitis autoinmune
- Reacción adversa a medicamentos
- Isquemia y perforación intestinal
- Malignidad hematológica
- Eritema multiforme
Patrones Moleculares Asociados a Patógenos (PAMP)
- Infección bacteriana
- Síndrome viral, como la gripe
- Infección fúngica diseminada en inmunodeprimidos
- Síndrome de shock tóxico derivado de exotoxinas y endotoxinas
Los PAMP también pueden clasificarse según la ubicación y el alcance de la diseminación de la infección, que va desde una infección localizada específica de un órgano hasta bacteriemia diseminada y sepsis.
Epidemiología
Una definición altamente sensible y menos específica del síndrome de respuesta inflamatoria sistémica resulta en una captura inexacta de la verdadera incidencia. No todos los pacientes con SIRS llegan a un centro de atención médica o son hospitalizados. Los médicos a menudo manejan síndromes virales agudos en la temporada alta en entornos de atención urgente y sala de emergencias con autocontención posterior. Solo aquellos que progresan en el continuo de gravedad son verdaderamente capturados en el censo de pacientes. Esto también refleja un sesgo en la gravedad y la mortalidad por todas las causas, así como en las medidas de resultado relacionadas.
En un estudio a gran escala que involucró a 269,951 pacientes hospitalizados, se encontró que el 15% de los pacientes cumplían al menos dos criterios diagnósticos para SIRS durante el ingreso, mientras que un abrumador 47% los cumplía al menos una vez durante la estancia hospitalaria. La tasa de mortalidad fue significativamente mayor en pacientes con SIRS (4.3%) que en aquellos sin SIRS (1.2%). Otro estudio reveló una incidencia hospitalaria general de 542 episodios por cada 1000 días de hospitalización.
Se demostró que el 62% de los pacientes que se presentaron en el departamento de emergencias con SIRS tenían una infección confirmada, mientras que dentro de la misma cohorte de pacientes, el 38% de los pacientes infectados no se presentaron con SIRS. En un estudio prospectivo de ingresos en un centro de atención terciaria, se mostró que el 68% de los ingresos hospitalarios en las unidades encuestadas cumplían los criterios SIRS. El 26% desarrolló sepsis, el 18% desarrolló sepsis grave y el 4% desarrolló shock séptico dentro de los 28 días posteriores al ingreso.
En cuanto a la variación entre sexo y raza, se ha observado un efecto protector del estrógeno en modelos animales con trauma, hemorragia y sepsis. Del mismo modo, se informó una menor incidencia de SIRS en mujeres y afroamericanos. Por razones comprensibles, los extremos de edad y las comorbilidades médicas concomitantes impactan negativamente el resultado del SIRS.
Fisiopatología
La inflamación desencadenada por un estímulo infeccioso o no infeccioso pone en marcha una compleja interacción de la respuesta inmune humoral y celular, citoquinas y la vía del complemento. Eventualmente, el síndrome de respuesta inflamatoria sistémica resulta cuando el equilibrio entre las cascadas proinflamatorias y antiinflamatorias se inclina hacia la primera. Se han descrito cinco etapas superpuestas de la cascada de la sepsis que comienza con SIRS y progresa a MODS (Síndrome de Disfunción Multiorgánica), si no se contrarresta adecuadamente por una respuesta antiinflamatoria compensatoria o la mitigación de la etiología incitante primaria.
Etapas Fisiopatológicas
Etapa 1: Reacción Local. Es una reacción local en el sitio de la lesión que tiene como objetivo contener la lesión y limitar su propagación. Las células efectoras inmunes en el sitio liberan citoquinas que a su vez estimulan el sistema reticuloendotelial, promoviendo la reparación de heridas a través de la inflamación local. Hay vasodilatación local inducida por óxido nítrico y prostaciclina (rubor) y disrupción de la unión estrecha endotelial para permitir la marginación y transferencia de leucocitos al espacio tisular. La fuga de células y líquido rico en proteínas en el espacio extravascular causa hinchazón (tumor) y aumento de calor (calor). Los mediadores inflamatorios impactan los nervios somatosensoriales locales causando dolor (dolor) y pérdida de función (functio laesa). Esa pérdida de función también permite que la parte del cuerpo se repare en lugar de un uso persistente.
Etapa 2: CARS Temprano. Es un síndrome de respuesta antiinflamatoria compensatoria temprana (CARS) en un intento de mantener el equilibrio inmunológico. Hay una estimulación de factores de crecimiento y reclutamiento de macrófagos y plaquetas a medida que el nivel de mediadores proinflamatorios disminuye para mantener la homeostasis.
Etapa 3: Predominio del SIRS. Es cuando la balanza se inclina hacia el SIRS proinflamatorio, lo que resulta en disfunción endotelial progresiva, coagulopatía y activación de la vía de la coagulación. Esto resulta en microtrombosis de órganos terminales y un aumento progresivo de la permeabilidad capilar, lo que eventualmente resulta en la pérdida de la integridad circulatoria.
Etapa 4: Predominio del CARS. Se caracteriza por el CARS tomando el control del SIRS, lo que resulta en un estado de inmunosupresión relativa. El individuo, por lo tanto, se vuelve susceptible a infecciones secundarias o nosocomiales, perpetuando así la cascada séptica.
Etapa 5: MODS. Se manifiesta en MODS con desregulación persistente de las respuestas tanto del SIRS como del CARS.
A nivel celular, estímulos nocivos no infecciosos, un agente infeccioso o una endotoxina o exotoxina producida por una infección activan una multitud de células, incluidos neutrófilos, macrófagos, mastocitos, plaquetas y células endoteliales. La respuesta temprana mediada por estas células inflamatorias implica tres vías principales:
- Activación de IL-1 y TNF alfa.
- Activación de la vía de prostaglandinas y leucotrienos.
- Activación de la vía del complemento C3a – C5a.
La interleucina 1 (IL1) y el factor de necrosis tumoral alfa (TNF-alfa) son los mediadores tempranos en la primera hora. Su papel es de suma importancia para inclinar la balanza hacia una sobrecarga proinflamatoria. Sus acciones pueden dividirse ampliamente en tres categorías:
- Propagación de la vía de las citoquinas.
- Alteración de la coagulación que causa anomalías microcirculatorias.
- Liberación de hormonas del estrés.
La liberación de IL1 y TNF-alfa resulta en la disociación del factor nuclear-kB (NF-kB) de su inhibidor. NF-kB puede así inducir la liberación masiva de otras citoquinas proinflamatorias, incluidas IL-6, IL-8 e Interferón gamma. La IL-6 induce la liberación de reactantes de fase aguda, incluida la procalcitonina y la proteína C reactiva. Los desencadenantes infecciosos tienden a producir un mayor aumento de TNF-alfa y, por lo tanto, de IL-6 e IL-8. Otra citoquina proinflamatoria potente es la proteína del grupo de alta movilidad box 1 (HMGB1), que está involucrada en la respuesta citotóxica tardía del SIRS y la sepsis. Se ha establecido como un predictor independiente de mortalidad a 1 año en un estudio observacional de pacientes con lesión cerebral traumática.
Al igual que la mayoría de las otras respuestas tempranas en el SIRS, la alteración de la vía de la coagulación también es desencadenada por IL-1 y TNF-alfa. La fibrinólisis se ve afectada por la activación del inhibidor del activador del plasminógeno-1. Hay lesión endotelial directa, lo que resulta en la liberación del factor tisular, que desencadena la cascada de la coagulación. Además, los mediadores antiinflamatorios Proteína C activada y antitrombina se inhiben. Como resultado, hay una trombosis microvascular generalizada, un aumento de la permeabilidad capilar, así como fragilidad y deterioro de la perfusión tisular, lo que contribuye a la disfunción orgánica progresiva.
Principalmente, las catecolaminas, la vasopresina y la activación del eje renina-angiotensina-aldosterona resultan en un aumento de la liberación de esteroides endógenos. Las catecolaminas son responsables del componente de taquicardia y taquipnea de la sepsis, mientras que los glucocorticoides contribuyen al aumento del recuento de leucocitos, así como a su marginación en la circulación periférica.
El Síndrome de Respuesta Antiinflamatoria Compensatoria (CARS) está mediado por las interleucinas IL-4 e IL-10, que tienden a inhibir la producción de TNF-alfa, IL-1, IL-6 e IL-8. El equilibrio entre SIRS y CARS decide dónde se encuentra el punto de terminación en el continuo de SIRS a MODS. El CARS tiene sus propios peligros. Si se permite que se perpetúe, somete al individuo sobreviviente a un estado prolongado de inmunosupresión. El individuo se vuelve así susceptible a infecciones nosocomiales, que pueden reiniciar la cascada séptica.
Evaluación y Biomarcadores
Con el tiempo, ha habido un cambio gradual de paradigma, pasando de basar el diagnóstico de sepsis únicamente en los clínicos a la incorporación de parámetros más objetivos. Si bien es incuestionablemente un diagnóstico clínico y no puede definirse simplemente por ensayos diagnósticos sin el reconocimiento de los signos por parte del clínico, la identificación rápida de criterios clínicos uniformes se volvió cada vez más importante. A medida que se hicieron nuevos avances a finales del siglo XX en la compleja fisiopatología, etiología y objetivos farmacoterapéuticos, la necesidad de un diagnóstico e intervención tempranos se hizo evidente para impactar la mortalidad y la morbilidad. El reconocimiento del continuo desde la inflamación temprana hasta la disfunción multiorgánica añadió más incentivo.
Así nació la necesidad de diagnosticar el síndrome de respuesta inflamatoria sistémica tanto en el contexto de la infección como en el estrés no infeccioso donde el cuerpo luego se vuelve susceptible a una infección secundaria. El establecimiento de criterios clínicos fue el esfuerzo inicial. Así nacieron las puntuaciones APACHE, SIRS, SOFA y qSOFA, LOD. Cada una de ellas evolucionó con la intención de encontrar un sistema de puntuación más simple, fácilmente aplicable y rápido que pueda usarse en cualquier entorno clínico para predecir:
- Identificación de sepsis.
- Riesgo de disfunción orgánica.
- Mortalidad hospitalaria.
Si la etiología del SIRS se identifica tempranamente, las investigaciones se individualizan al órgano en cuestión. En ausencia de una fuente aparente, la búsqueda sensible al tiempo de fuentes infecciosas se convierte en una prioridad. Los centros de atención médica y las guías de sociedades respaldan la recolección rutinaria de especímenes de sangre, esputo, orina y cualquier otra herida obvia para cultivo dentro de la primera hora de evaluación y antes de iniciar la terapia antimicrobiana. Dependiendo de la gravedad de la presentación, las investigaciones rutinarias implican la evaluación periódica del panel metabólico básico y el nivel de ácido láctico para evaluar el alcance de la lesión orgánica terminal y el deterioro de la perfusión.
Con el tiempo, también ha surgido una discusión en la comunidad sobre la importancia de distinguir la sepsis más tempranamente en el SIRS con la ayuda de biomarcadores, incluso antes de que los cultivos microbianos sean positivos. Los biomarcadores también son importantes para identificar el SIRS debido a una infección secundaria en pacientes que fueron admitidos inicialmente con una etiología no infecciosa, por ejemplo, trauma o quemaduras, o para una intervención quirúrgica planificada. Los meros criterios clínicos no son suficientes para capturar el cambio en la etiopatogenia a mitad de la hospitalización.
Biomarcadores
Procalcitonina (PCT): Un precursor glicoproteico de la calcitonina, la procalcitonina es producida por las células C del timo y también por leucocitos, hígado, riñón, tejido adiposo y muscular. En individuos sanos, los niveles séricos suelen estar por debajo de 0.1 mg/dl, pero pueden ser significativamente anormales en infecciones bacterianas, fúngicas o parasitarias. Los niveles pueden elevarse ligeramente en infecciones virales o inflamación aguda no infecciosa y también pueden aumentar en individuos con tumores neuroendocrinos o estrés postquirúrgico. Las concentraciones séricas aumentan dentro de 2 a 4 horas del pico inflamatorio y caen rápidamente después de detener el insulto primario. La vida media es de aproximadamente 25 a 30 horas. La concentración sérica máxima, por lo tanto, parece paralelizar el cronograma de la gravedad y el resultado de la enfermedad. La investigación se ha centrado principalmente en la utilidad de la procalcitonina para diferenciar la causa infecciosa de la no infecciosa del SIRS y su valor en la evaluación serial para determinar la duración de la terapia antimicrobiana. Se ha demostrado que la procalcitonina es favorable sobre la PCR en el diagnóstico y pronóstico de la sepsis, pero solo en conjunto con parámetros clínicos. También se ha confirmado su valor en la predicción de un proceso infeccioso sistémico, aunque el valor de corte parece diferir según el proceso de la enfermedad. En una comparación de una amplia gama de biomarcadores en pacientes con trauma, solo la procalcitonina fue beneficiosa para predecir la sepsis. Los niveles persistentemente altos se correlacionaron bien con un aumento de la mortalidad y las puntuaciones de gravedad. Las mediciones seriales de PCT en la UCI contribuyeron a una reducción significativa de los días de estancia en la UCI y la duración de la terapia antimicrobiana. Las concentraciones plasmáticas de procalcitonina (PCT), C3a e IL-6 obtenidas hasta 8 horas después del inicio clínico de la sepsis o el SIRS fueron significativamente más altas en pacientes con etiologías infecciosas. PCT, IL-6 y C3a fueron más fiables para distinguir SIRS de sepsis.
Lactato: La elevación del ácido láctico puede ser una acidosis láctica tipo A con producción excesiva debido al metabolismo anaeróbico relacionado con la hipoperfusión tisular o acidosis láctica tipo B por aclaramiento inadecuado debido a disfunción hepática. El uso de epinefrina como agente vasopresor también puede conducir a una producción excesiva de lactato debido a la alteración del ciclo del piruvato.
Interleucina 6: Un nivel de IL-6 superior a 300 pg/ml se correlaciona con una mayor incidencia de MODS y muerte. Del mismo modo, se ha demostrado que una reducción en el nivel al segundo día de terapia antimicrobiana es un signo pronóstico positivo.
Leptina: Los niveles séricos de leptina superiores a un punto de corte de 38 mcg/L correlacionan los niveles séricos de IL-6 y TNF-alfa y ayudan a diferenciar entre causas infecciosas y no infecciosas de SIRS con una sensibilidad del 91.2% y una especificidad del 85%. Es una hormona de acción central generada por adipocitos que actúa sobre el hipotálamo.
Marcadores Endoteliales: La angiopoyetina 1 y 2 son ligandos para el receptor Tie-2 en las células endoteliales. Hay un aumento de la unión de la angiopoyetina 2 (Ang-2) con el receptor Tie-2, lo que desencadena la trombosis microvascular y la permeabilidad capilar durante la inflamación aguda. Los niveles circulantes de Ang-2 parecen correlacionarse con la mortalidad a los 28 días en SIRS y las puntuaciones de gravedad como APACHE y SOFA. Se ha atribuido una significancia similar a los niveles solubles de E-selectina y P-selectina, que pueden ayudar a distinguir entre etiologías sépticas y no sépticas del SIRS. En un estudio de 92 pacientes con SIRS, se encontró que la E-selectina soluble era más útil para identificar el SIRS temprano y pronosticar la gravedad. La molécula de adhesión intracelular soluble (s-ICAM 1) ayudó a distinguir a los pacientes sépticos y no sépticos. Sin embargo, ninguno de sus métodos analíticos está estandarizado y aún no se han establecido niveles de corte para introducirlos en el mercado pronto.
Biomarcadores Emergentes: Otros biomarcadores emergentes en investigación para distinguir la etiología séptica y no séptica del SIRS incluyen el receptor desencadenante expresado en células mieloides 1 (TREM-1), el receptor señuelo 3 (DcR3) (pertenece a la familia del factor de necrosis tumoral) y el suPAR (receptor soluble del activador del plasminógeno de tipo uroquinasa). Entre ellos, el suPAR se correlacionó particularmente bien con las puntuaciones de gravedad de la enfermedad y la identificación de no sobrevivientes en el grupo de sepsis.
Análisis de Transcriptoma: Ha habido una idea emergente detrás de la fisiopatología del SIRS en los últimos años que sugiere la desregulación inmune como un fenómeno clave más que un simple aumento inflamatorio en el SIRS y la sepsis. Utilizando la secuenciación de alto rendimiento de ADNc de células mononucleares, se ha identificado un perfil genético de tolerancia a endotoxinas (llamado firma de tolerancia a endotoxinas o ETS), que se expresa con mayor frecuencia en pacientes sépticos y se asoció más comúnmente con falla orgánica y gravedad de la enfermedad. Por lo tanto, puede proporcionar una oportunidad para identificar tempranamente una subpoblación de pacientes sépticos para el ingreso en la UCI y la terapia intensiva, impactando la mortalidad y la morbilidad.
Tratamiento y Manejo
El síndrome de respuesta inflamatoria sistémica es una conglomeración de manifestaciones clínicas de una causa desencadenante; el manejo se centra en tratar la condición desencadenante primaria. Por lo tanto, el manejo se diseña en torno a una búsqueda paralela de la etiología subyacente y su resolución, junto con intervenciones sensibles al tiempo que pueden no ser específicas de la causa, pero que se dirigen a prevenir la lesión orgánica terminal. El objetivo es interrumpir la progresión a lo largo del continuo del shock y el síndrome de disfunción multiorgánica.
Garantizar la estabilidad hemodinámica es de suma importancia. En sepsis grave y shock séptico, las guías de manejo de sepsis recomiendan una administración inicial de cristaloides isotónicos a una velocidad de bolo de 30 ml/kg. Establecer arbitrariamente estándares de volumen en todo el espectro de pacientes con reserva cardíaca, renal y de proteínas intravasculares variable puede ser un tema de debate clínico. Por lo tanto, algunos estándares de práctica son consistentes con la administración de volumen posterior guiada por medidas dinámicas de respuesta al volumen. Para un paciente que respira espontáneamente y no presenta arritmia cardíaca, los índices utilizados incluyen la medición de la variabilidad de la presión del pulso o la variabilidad del volumen sistólico con elevación pasiva de las piernas. Para un paciente con soporte de ventilación mecánica, la variabilidad de la presión del pulso, la variabilidad del volumen sistólico o la variabilidad del diámetro de la vena cava inferior con la respiración son una opción.
Los vasopresores e inotrópicos son útiles en el shock que no responde a la reposición de volumen. Una descripción detallada de su uso se encuentra dentro del ámbito de la discusión del manejo del shock en específico.
El control de la fuente primaria puede implicar una intervención quirúrgica, por ejemplo, incisión y drenaje de una infección de herida, drenaje con tubo de un absceso o colección contenida, o cirugía exploratoria. Cuando el clínico sospecha que la sepsis es la causa del SIRS, y en individuos predispuestos específicos, por ejemplo, debilidad generalizada, inmunosupresión, neutropenia o asplenia, se indica una terapia antibiótica empírica de amplio espectro inmediatamente después de la recolección de muestras para cultivo.
Los antibióticos de amplio espectro deben guiarse por:
- Sospecha de infección adquirida en la comunidad vs. hospitalaria.
- Patrones microbiológicos previos en el individuo.
- Antibiograma del centro.
Se recomienda la desescalada rápida una vez que los resultados del cultivo estén disponibles. La terapia antiviral se considera solo con exacerbación respiratoria y síndrome de respuesta inflamatoria sistémica en la temporada de influenza. Los pacientes neutropénicos y aquellos con nutrición parenteral total con acceso venoso central pueden necesitar antifúngicos empíricos si continúan mostrando respuesta SIRS después de los antibióticos empíricos.
Se ha demostrado que los glucocorticoides en dosis bajas (200 a 300 mg de hidrocortisona o equivalente) mejoran la supervivencia y ayudan a revertir el shock en pacientes con shock persistente a pesar de la reanimación con líquidos y el uso de vasopresores. No hay evidencia en el nivel de cortisol sérico o en las pruebas de estimulación con ACTH para determinar la indicación de esteroides en el shock séptico. La razón es una disminución de la respuesta a nivel del receptor en lugar de una reducción absoluta en el nivel de cortisol sérico como causa de insuficiencia suprarrenal relativa en los síndromes SIRS.
Control de la glucosa en sangre: En un estudio histórico en pacientes de UCI quirúrgica, se informó una reducción de las tasas de mortalidad hospitalaria con terapia intensiva con insulina (mantenimiento de la glucosa en sangre entre 80 y 110 mg/dL) en un 34%. Sin embargo, posteriormente, el gran ensayo NICE-SUGAR no logró replicar el beneficio en el resultado del control estricto de la glucosa, con una mayor incidencia de complicaciones de hipoglucemia e hipokalemia. Las guías de manejo de sepsis recomiendan el control de la glucosa en sangre a menos de 180 mg/dl.
Diagnóstico Diferencial
El síndrome de respuesta inflamatoria sistémica, al ser una definición altamente sensible, con la necesidad de satisfacer solo dos de cuatro criterios, conlleva la pérdida inevitable de especificidad. Una combinación de dos criterios SIRS puede reflejar una serie de presentaciones clínicas en un entorno agudo, que pueden no reflejar un estado inflamatorio subyacente que el SIRS significa. Algunos comunes incluyen:
Taquipnea y Taquicardia
- Estado asmático agudo con administración frecuente de agonistas beta.
- Toxicidad aguda por salicilatos.
- Intoxicación aguda por alcohol.
- Cetoacidosis aguda (diabética, por inanición, por deshidratación).
- Ataque de pánico.
Taquicardia con Hipertermia
- Crisis tirotóxica.
- Intoxicación aguda por abuso de sustancias (alucinógenos, estimulantes psicotrópicos).
- Síndrome serotoninérgico.
- Hipertermia maligna.
- Síndrome neuroléptico maligno.
Hipertermia y Leucocitosis
- Emergencia neurogénica con accidente cerebrovascular hemorrágico agudo (pontino).
La presencia sostenida de criterios clínicos a lo largo del tiempo con evaluación a intervalos repetidos, así como la corroboración con índices de laboratorio, ayudan a distinguirlos de un medio inflamatorio.
Pronóstico
Una puntuación de síndrome de respuesta inflamatoria sistémica de 2 o más en el día 1 de hospitalización tiene más probabilidades de desarrollar síndrome de disfunción multiorgánica (MODS), tener una estancia más prolongada en la UCI y tener una mayor necesidad de ventilación mecánica, soporte vasopresor, sangre y productos sanguíneos. El intervalo de tiempo medio desde SIRS hasta sepsis en el continuo está inversamente relacionado con el número de criterios SIRS cumplidos al ingreso.
Curiosamente, las tasas de mortalidad en un estudio fueron del 7% (SIRS), 16% (sepsis), 20% (sepsis grave) y 46% (shock séptico). Mientras que en un estudio similar sobre mortalidad hospitalaria, se informaron tasas de mortalidad del 1.3% (sepsis), 9.2% (sepsis grave) y 28% (shock séptico). La diferencia refleja un cambio en los patrones de práctica durante una década, con una mayor adherencia a la terapia temprana dirigida por objetivos y el uso de enfoques probados de reducción de riesgos como la profilaxis de TVP, el control de la glucosa en sangre, el volumen corriente protector pulmonar en la ventilación mecánica, el despertar diario y la deambulación temprana.
Otra observación interesante fue que la presencia de criterios SIRS por sí sola no se correlacionó con la mortalidad hospitalaria o a 1 año. La disfunción orgánica resultó ser un mejor predictor de mortalidad, validando así la importancia de las puntuaciones SOFA y qSOFA.
Complicaciones
Las complicaciones del síndrome de respuesta inflamatoria sistémica pueden incluir la progresión del estado de la enfermedad a lo largo del continuo de sepsis (para etiología infecciosa) a sepsis grave, a shock y a síndrome de disfunción multiorgánica. Las complicaciones también pueden estar relacionadas con la disfunción orgánica individual. Algunas importantes son las siguientes:
- Sistema Nervioso Central: Encefalopatía aguda.
- Sistema Respiratorio: Síndrome de dificultad respiratoria aguda (SDRA), neumonitis por aspiración aguda relacionada con la encefalopatía.
- Sistema Cardíaco: Desajuste entre la demanda y la perfusión que causa elevación de troponina, taquiarritmia.
- Sistema Gastrointestinal: Úlcera por estrés, transaminitis aguda.
- Sistema Renal: Necrosis tubular aguda y lesión renal aguda, acidosis metabólica, anomalías electrolíticas.
- Sistema Hematológico: Trombocitosis o trombocitopenia, coagulación intravascular diseminada, hemólisis, trombosis venosa profunda.
- Sistema Endocrino: Hiperglucemia, insuficiencia suprarrenal aguda.
Educación del Paciente y Prevención
Siendo el tiempo de suma importancia en el resultado del SIRS y la sepsis, la identificación temprana es clave para un resultado favorable. La educación y la concienciación entre los pacientes predispuestos y las familias cuidadoras sobre los signos de alerta temprana deben ser una prioridad. Un subgrupo relevante es el de los individuos con inmunosupresión primaria o adquirida subyacente. Durante el manejo, educar a los familiares cercanos y a los pacientes que pueden participar, sobre el pronóstico individualizado, las complicaciones, los beneficios y riesgos del tratamiento ayuda a mitigar la respuesta al estrés simpático perjudicial. También es importante evaluar la capacidad de afrontamiento y la aprehensión del paciente/familiar con respecto a las intervenciones diagnósticas y terapéuticas con las que no están familiarizados.
El Equipo de Atención Médica
A medida que se realizan nuevos avances hacia la comprensión de esta compleja fisiopatología, etiología y objetivos farmacoterapéuticos del SIRS y la sepsis, la carrera contra el tiempo para la identificación temprana de individuos propensos a manifestaciones de enfermedad más graves es ahora la prioridad. Junto con la utilización de una definición clínica altamente sensible para identificar al paciente susceptible, se están considerando nuevas puntuaciones clínicas e índices de laboratorio para separar rápidamente las etiologías infecciosas de las no infecciosas e identificar tempranamente el riesgo de disfunción orgánica y muerte.
Una intervención orquestada y sensible al tiempo implica una ejecución rápida y efectiva desde el nivel de triaje hasta la sala de emergencias y la unidad de cuidados intensivos, todos funcionando como un equipo interprofesional cohesionado. Probablemente comienza incluso antes en individuos susceptibles en el punto de reconocimiento temprano de la inestabilidad por sí mismos o por la familia con educación y concienciación adecuadas. Dada la complejidad del diagnóstico y la gravedad de la afección, el diagnóstico y manejo del síndrome de respuesta inflamatoria sistémica requiere un enfoque de equipo interprofesional. Una variedad de clínicos, incluyendo médicos de atención primaria/familiar, especialistas en diversas áreas (hematología, enfermedades infecciosas), personal de enfermería especializado y farmacéuticos, deben hacer contribuciones únicas al manejo de estos pacientes.
Las intervenciones del clínico han sido objeto de gran parte de este artículo. El personal de enfermería a menudo tendrá la responsabilidad de monitorizar al paciente y administrar los medicamentos necesarios para estabilizarlo. Dada la amplia variedad de medicamentos que pueden ser necesarios, se debe consultar a los farmacéuticos para garantizar los regímenes de dosificación adecuados y evaluar el potencial de interacciones medicamentosas, poniéndose a disposición tanto de los clínicos como del personal de enfermería para ayudar con la coordinación de la atención y la educación del paciente. Todos los miembros del equipo deben registrar sus hallazgos y mantener líneas abiertas de comunicación para consultas e informes, de modo que todos en el equipo de atención operen desde la misma base de información. Solo a través de este tipo de paradigma interprofesional colaborativo pueden estos pacientes recibir la terapia oportuna y adecuada que necesitan.
Los sistemas de puntuación uniformes respaldados por sociedades clínicas y los programas y paquetes de sepsis o SIRS a nivel hospitalario brindan uniformidad a las intervenciones. La mayoría de los sistemas hospitalarios han estado utilizando listas de verificación y las han incorporado en sus medidas de control de calidad para lograr la perfección en la ejecución. La supervisión de CMS/Medicare del rendimiento del sistema de atención médica ha añadido un incentivo al esfuerzo y abre nuevos debates y discusiones para la improvisación.
Preguntas Frecuentes (FAQ)
- ¿Qué es el Síndrome de Respuesta Inflamatoria Sistémica (SIRS)?
Es una respuesta de defensa exagerada del cuerpo ante un factor estresante nocivo, como una infección o un trauma, con el objetivo de localizar y eliminar la fuente del problema. - ¿Cómo se define objetivamente el SIRS?
Se define por la presencia de al menos dos de los siguientes criterios: temperatura anormal, frecuencia cardíaca elevada, frecuencia respiratoria elevada o pCO2 baja, o recuento anormal de leucocitos. - ¿Es lo mismo SIRS que Sepsis?
No exactamente. La sepsis se define como SIRS con una fuente de infección sospechada. Casi todos los pacientes sépticos tienen SIRS, pero no todos los pacientes con SIRS son sépticos. - ¿Por qué se crearon los criterios SIRS?
Se crearon a principios de los años 90 para identificar de manera temprana a pacientes con respuestas inflamatorias generalizadas, con el fin de mejorar el diagnóstico y manejo temprano de condiciones graves como la sepsis. - ¿Qué son los biomarcadores y por qué son importantes en SIRS?
Son sustancias medibles en el cuerpo que pueden indicar la presencia, gravedad o pronóstico de una condición. En SIRS, biomarcadores como la procalcitonina son importantes para ayudar a diferenciar causas infecciosas de no infecciosas y predecir resultados. - ¿Cómo se trata el SIRS?
El manejo se centra en tratar la causa subyacente (como una infección o trauma) y en estabilizar al paciente, a menudo con fluidos, vasopresores y, si se sospecha infección, antibióticos. - ¿Cuáles son las posibles complicaciones del SIRS?
Las complicaciones pueden incluir la progresión a sepsis grave, shock séptico y síndrome de disfunción multiorgánica (MODS), así como disfunciones específicas de órganos como SDRA, lesión renal aguda o coagulación intravascular diseminada.
Si quieres conocer otros artículos parecidos a Entendiendo los Criterios SIRS puedes visitar la categoría Sofas.